Результаты исследований могут иногда приходить из неожиданных мест. Например, по данным Parkinson’s News Today, преимущества и недостатки исследуемой генной терапии были изучены в результате посмертного анализа двух пациентов с болезнью Паркинсона.
Терапия, CERE-120, доставляет ген нейротурина (NRTN) в мозг. Следует признать, что это имело мало терапевтических преимуществ во время клинических испытаний. Тем не менее, исследователи считают, что долгосрочный посмертный анализ мозга показывает, где можно улучшить терапию для повышения эффективности в будущем. Читайте полный текст исследования в журнале Brain здесь.
Что такое болезнь Паркинсона?
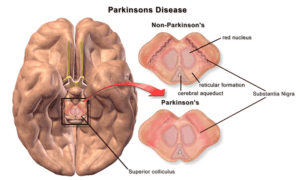
Болезнь Паркинсона — это прогрессирующее расстройство центральной нервной системы, которое происходит в пять этапов:
- Легкие симптомы и легкий тремор
- Более заметные симптомы с легким тремором и мышечной ригидностью
- Потеря баланса и замедленное движение
- Сильные симптомы, которые мешают самостоятельной жизни
- Пациенты теряют способность стоять и ходить, могут возникнуть галлюцинации
Более ранние симптомы включают тремор или тряску, особенно в руках, наряду с жесткими мышцами, нарушение баланса и речевые изменения. Болезнь Паркинсона возникает, когда нервные клетки мозга дегенерируют, умирают или каким-либо образом повреждаются. Эти нервные клетки создают дофамин, который обычно помогает передавать сообщения мышцам. Без этого ценного дофамина моторная функция снижается. Узнайте больше о болезни Паркинсона на нашем сайте.
Генная Терапия
CERE-120
CERE-120 была впервые разработана биотехнологической компанией Ceregene. Эта исследовательская генная терапия была направлена на защиту нейронов мозга, пораженных болезнью Паркинсона. CERE-120 работает путем доставки нейротурина (NRTN) непосредственно в две области головного мозга: путамен и черную субстанцию. Они известны своей ролью в передвижении. NRTN особенно борется с нейродегенерацией.
Эта терапия имела противоположные результаты в опытах на животных и людях. На животных моделях болезни Паркинсона аденоассоциированный вирус серотипа 2 имплантировал NRTN в мозг. Исследователи обнаружили, что нейроны, связанные с дофамином, были защищены, увеличивая производство дофамина.
После результатов испытаний на животных исследователи перешли к открытому первому этапу клинического испытания. Это было изначально многообещающим. Пациенты с болезнью Паркинсона хорошо переносили терапию, предполагая, что она безопасна для применения. Это испытание также обнаружило некоторое улучшение симптомов. В то же время двойное слепое исследование второго этапа показало, что CERE-120 не оказал реального влияния на пациентов по сравнению с пациентами, которым не давали CERE-120.
Следующее исследование стремилось доставить более высокую дозу CERE-120 в путамен и окружающую черную субстанцию. Еще раз, пациенты не показали улучшения симптомов.
Исследования Пациентов После Смерти
Исследователи хотели понять, почему успешные результаты клинического испытания первого этапа не были подтверждены в дальнейших исследованиях. Поэтому они провели дополнительные посмертные (после смерти) анализы двух пациентов с болезнью Паркинсона, которые участвовали в клинических испытаниях CERE-120.
Пациенты
Первый пациент был вовлечен в первый этап второго исследования CERE-120, которое имплантировало терапию только в путамен. Пациент прожил десять лет после операции.
Второй пациент был вовлечен во второй этап второго исследования CERE-120, которое имплантировало терапию как в путамен, так и в черную субстанцию. Пациент прожил восемь лет после операции.
Чтобы гарантировать точность своих исследований, ученые также исследовали мозг еще четырех человек. Двое были пациентами с болезнью Паркинсона примерно того же возраста, что и пациенты 1 и 2. Они не проходили генную терапию. Последние два изученных мозга были от двух людей того же возраста, у которых не было неврологических заболеваний, включая болезнь Паркинсона.
Выводы
Оба пациента, и 1 и 2, продемонстрировали продукцию NRTN в путамене. Их мозг также имел повышенные ферменты тирозингидроксилазы (TH); это является ключевым, потому что этот фермент действительно помогает производить дофамин. В то время как оба пациента демонстрировали ферменты TH, они были выше у Пациента 2. Это говорит о том, что терапия могла бы быть более эффективной, если бы она доставлялась в несколько областей головного мозга, в отличие от одной единичной доставки.
Исследователи обнаружили NRTN в 19% оставшихся дофаминергических (связанных или производящих дофамин) нейронов в мозге пациента 1. Мозг пациента 2 показал NRTN в 39% оставшихся нейронов. Оставшиеся четыре мозга не показали NRTN.
Рецептор, называемый RET, также был обнаружен в более высокой концентрации в головном мозге пациента 2, чем пациента 1. Некоторые предшествующие исследования предполагают, что накопление альфа-синуклеиновых белков, которое происходит при болезни Паркинсона, может прерывать RET и останавливать продукцию NRTN.
В конечном итоге, это исследование открывает двери для новых соображений. В настоящее время генная терапия CERE-120 может не обеспечить достаточного количества NRTN для лечения болезни Паркинсона. Тем не менее, посмертные исследования показывают, что генная терапия может способствовать долгосрочному производству TH у пациентов. Если исследователи смогут найти способы увеличить это производство и быстрее увидеть результаты, генная терапия может стать эффективным лечением для пациентов с болезнью Паркинсона.